Université de Haïfa : un mécanisme de communication cellulaire pourrait expliquer l’échec de certains traitements contre le cancer

Le récepteur Notch, jusqu’ici considéré comme un simple récepteur de signaux, agit comme une molécule de signalisation qui active les cellules voisines et peut même les inciter à phagocyter des cellules vivantes. Les résultats de cette étude pourraient modifier notre compréhension des maladies associées à Notch, notamment certains cancers, et expliquer pourquoi les traitements ciblant uniquement l’activité intracellulaire n’ont jusqu’à présent pas donné de résultats significatifs.
Une étude menée à l’Université de Haïfa a révélé qu’un mécanisme central de communication intercellulaire fonctionne différemment qu’on ne le pensait jusqu’ici. Cette découverte pourrait expliquer l’échec, jusqu’à présent, des traitements contre des maladies graves, dont certains cancers. L’étude porte sur le récepteur Notch, une protéine essentielle à la communication intercellulaire, déjà impliquée dans diverses maladies, dont plusieurs types de cancer.
Contrairement à l’hypothèse selon laquelle Notch ne fonctionne que comme récepteur de signaux provenant d’autres cellules, les chercheurs ont démontré que ce récepteur est également capable d’agir comme un signal activant des récepteurs sur des cellules voisines, voire de les inciter à phagocyter des cellules vivantes. Il s’agit d’un changement fondamental dans la compréhension scientifique de l’activité de Notch. « Le nouveau mécanisme que nous avons identifié pourrait expliquer pourquoi les traitements ciblant uniquement l’activité intracellulaire n’ont jusqu’à présent pas donné de résultats significatifs, puisque le récepteur Notch agit également comme un signal vers les cellules voisines et influence ces dernières », explique la Pr Hila Toledano de l’Université de Haïfa, co-auteure de l’étude.
 La communication intercellulaire est un processus biologique essentiel qui permet aux cellules d’échanger des informations et de coordonner des activités complexes au sein des tissus et des organes. Dans ce processus, les cellules « transmettent » des signaux moléculaires qui sont reçus par d’autres cellules via des récepteurs spécifiques situés à la surface de leur membrane. Lorsqu’un tel signal se lie à un récepteur, il modifie l’activité de la cellule réceptrice et affecte ainsi sa fonction, son état, voire son devenir. Ce mécanisme est essentiel à la régulation précise de processus tels que le développement embryonnaire, la différenciation cellulaire et le maintien de l’équilibre tissulaire. L’un des récepteurs centraux de cette communication est le récepteur Notch, identifié pour la première fois il y a plus d’un siècle chez la drosophile.
La communication intercellulaire est un processus biologique essentiel qui permet aux cellules d’échanger des informations et de coordonner des activités complexes au sein des tissus et des organes. Dans ce processus, les cellules « transmettent » des signaux moléculaires qui sont reçus par d’autres cellules via des récepteurs spécifiques situés à la surface de leur membrane. Lorsqu’un tel signal se lie à un récepteur, il modifie l’activité de la cellule réceptrice et affecte ainsi sa fonction, son état, voire son devenir. Ce mécanisme est essentiel à la régulation précise de processus tels que le développement embryonnaire, la différenciation cellulaire et le maintien de l’équilibre tissulaire. L’un des récepteurs centraux de cette communication est le récepteur Notch, identifié pour la première fois il y a plus d’un siècle chez la drosophile. Chez l’humain, des perturbations de cette voie de signalisation ont été associées à de nombreuses maladies, dont certains cancers, le syndrome d’Alagille et le CADASIL. Dans ce contexte, Heba Abo Romi et Neven Serhan, doctorants au sein du laboratoire de la professeure Hila Toledano, au département de biologie humaine de l’université de Haïfa, ont cherché à déterminer si le récepteur Notch fonctionne uniquement comme un récepteur recevant des signaux d’autres cellules, ou s’il joue un rôle supplémentaire dans la communication cellulaire. Les chercheurs ont utilisé un modèle de recherche chez la drosophile, permettant un suivi très précis des processus cellulaires. Ils ont combiné des méthodes avancées d’imagerie en temps réel, de marquage fluorescent pour identifier les cellules vivantes et mortes, et de manipulations génétiques permettant de moduler l’expression du récepteur Notch dans les cellules. Ils ont également comparé différentes versions de la protéine, y compris celles dépourvues du domaine intracellulaire responsable de la signalisation classique, et examiné l’impact de ces modifications sur le comportement cellulaire.
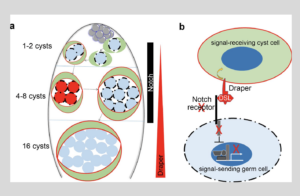
Les résultats de l’étude montrent que le récepteur Notch ne fonctionne pas uniquement comme récepteur de signaux, mais aussi comme signal activant les cellules voisines. Il apparaît que Notch se lie directement à un récepteur appelé Draper dans les cellules adjacentes, activant ainsi un processus d’englobement des cellules vivantes par ces dernières, un processus connu sous le nom de phagoptose. De façon surprenante, ce processus ne dépend pas de l’activité de signalisation intracellulaire de Notch, mais se produit même lorsque ce domaine est inactif. Ceci démontre que son activité de signalisation aux cellules voisines est indépendante du mécanisme de signalisation connu de Notch.
L’étude a également révélé qu’une augmentation des niveaux de Notch dans les cellules entraînait une augmentation significative de la mort cellulaire, tandis qu’une réduction de ces niveaux diminuait le processus ; en l’absence du récepteur Draper, le processus est totalement inhibé. Ces découvertes remettent en question notre compréhension fondamentale du sens de la signalisation cellulaire. « Ces résultats suggèrent un changement de paradigme dans la communication intercellulaire et dans l’interprétation des maladies associées à Notch. Si ce mécanisme existe également dans les maladies causées par des mutations de Notch, il est possible que les traitements ciblant uniquement son activité intracellulaire soient inefficaces, et que le sens de la signalisation et les récepteurs impliqués dans la maladie doivent être réexaminés », concluent les chercheurs.
Traduction/adaptation par Esther Amar pour Israël Science Info