UHJ (Israël) et Bristol U. : découverte d’un mécanisme de réécriture des messages génétiques par les cellules cancéreuses
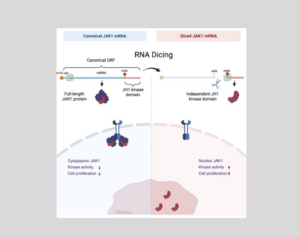
Des scientifiques ont mis au jour un mécanisme inattendu permettant aux cellules de générer des protéines oncogènes : le découpage de l’ARN en fragments fonctionnels plus courts, au lieu de suivre le schéma classique. Ce processus, récemment baptisé « découpage de l’ARN », permet la production d’une forme tronquée de la protéine JAK1, qui conserve une activité élevée et peut favoriser la croissance tumorale, notamment lorsque la fonction normale des gènes est perturbée. Cette découverte remet en question les conceptions classiques de la traduction de l’information génétique et révèle un mécanisme jusqu’alors inconnu, susceptible d’influencer la progression du cancer et la réponse aux thérapies ciblées. Le processus par lequel les cellules transforment les gènes en protéines était considéré depuis longtemps comme précis et étroitement régulé. Or, de nouvelles recherches montrent que les cellules peuvent, de manière inattendue, découper l’ARN en fragments plus courts qui produisent néanmoins des protéines fonctionnelles, parfois avec des conséquences néfastes.
Une équipe dirigée par le Dr Yuval Malka de l’Université hébraïque de Jérusalem et le Dr William Faller de l’Université de Bristol décrit un mécanisme jusqu’alors méconnu, qu’ils nomment «découpage de l’ARN ». Ce processus consiste à fragmenter les molécules d’ARN en fragments plus courts, capables de produire des protéines fonctionnelles et potentiellement nocives. Leur étude porte sur le gène JAK1, connu depuis longtemps pour son rôle central dans la régulation de la croissance, de la division et de la réponse immunitaire des cellules. Lorsque JAK1 fonctionne normalement, il contribue au maintien de l’équilibre cellulaire. Mais lorsqu’il dysfonctionne, il peut favoriser le développement du cancer. L’équipe a découvert que JAK1 ne produit pas une seule protéine, comme on le supposait auparavant. Son ARN peut être « découpé » en une forme plus courte, générant un fragment protéique tronqué mais toujours actif, véritable moteur de la molécule : le domaine kinase JH1.
Cette version tronquée fonctionne différemment de la protéine complète et peut induire une croissance cellulaire incontrôlée. « Nous constatons que le mécanisme de synthèse protéique cellulaire est bien plus flexible et dynamique que nous le pensions », suggèrent les chercheurs. «L’ARN n’est pas qu’un simple messager passif. Il peut être remodelé de manière à modifier la nature des protéines produites et leur comportement. » Les implications pour le cancer sont importantes. L’étude a révélé que l’équilibre entre la protéine JAK1 complète et sa forme tronquée peut influencer la capacité des cellules à rester sous contrôle ou à devenir tumorigènes. En particulier, certaines mutations, dites mutations non-sens, semblent perturber cet équilibre.
Ces mutations désactivent la forme normale de JAK1, suppressive des tumeurs, tout en amplifiant l’activité de la forme plus courte, pro-tumorale. Dans les cancers de l’endomètre, ce déséquilibre pourrait expliquer l’agressivité de certaines tumeurs. Mais ces résultats ouvrent également une perspective prometteuse. Les patientes dont les tumeurs présentent ces mutations, et dépendent donc davantage de la forme tronquée de JAK1, pourraient être particulièrement sensibles au Momelotinib, un médicament ciblant l’activité de JAK1. Autrement dit, le mécanisme même qui contribue à la progression du cancer pourrait aussi révéler une vulnérabilité. Cela ouvre la voie à des stratégies thérapeutiques plus précises, où les patients sont orientés vers des traitements adaptés non seulement aux gènes mutés, mais aussi à la manière dont ces gènes sont traités au niveau de l’ARN.
Au-delà de JAK1, cette découverte témoigne d’un changement plus profond dans la compréhension de l’expression génique. Pendant des décennies, on a cru que le nombre de protéines qu’une cellule pouvait produire était limité par ses gènes, mais des mécanismes comme le clivage de l’ARN suggèrent que le protéome est bien plus vaste et dynamique. Cette perspective permet également d’aborder l’une des questions les plus complexes de la recherche sur le cancer : comment un même gène peut-il jouer des rôles opposés dans la maladie ? Dans certains contextes, un gène agit comme un suppresseur de tumeur, tandis que dans d’autres, il favorise la croissance tumorale en tant qu’oncogène. Le clivage de l’ARN révèle une étape clé de ce processus, montrant comment un seul ARNm peut être traité de différentes manières, modifiant sa traduction et pouvant potentiellement faire basculer sa fonction de protectrice à nocive.
Ces découvertes commencent déjà à avoir des applications concrètes. Elles ont permis le dépôt d’un brevet pour une nouvelle approche thérapeutique basée sur le clivage de l’ARN et ont conduit à la création d’une entreprise de biotechnologie qui a obtenu un financement initial et se prépare aux essais précliniques. « Ceci ajoute une nouvelle dimension à la complexité du vivant», conclut l’étude. « Le traitement de l’ARN peut générer des protéines fonctionnelles entièrement nouvelles, avec des conséquences réelles sur les maladies. » À mesure que les chercheurs explorent cette dimension jusqu’alors insoupçonnée de la régulation génique, il devient de plus en plus évident que les mécanismes qui régissent l’interprétation de l’information génétique par les cellules sont bien plus complexes qu’on ne le pensait. Dans le cas du cancer, ces processus nouvellement identifiés pourraient jouer un rôle déterminant dans l’évolution de la maladie et dans l’élaboration de stratégies thérapeutiques plus précises et efficaces.
Institutions : Division d’oncogénomique, Institut néerlandais du cancer Département de biochimie et de biologie moléculaire, Institut de recherche médicale Israël-Canada, Faculté de médecine, Université hébraïque de Jérusalem Centre de recherche intégrative en chimie et biologie, Institut coréen des sciences et technologies Plateforme de protéomique NKI, Institut néerlandais du cancer Division des sciences biomédicales Technologie, École KIST, Université coréenne des sciences et technologies École de biochimie et de sciences biomédicales, Université de Bristol.